患者男,43 歲,因左足后跟外側無明顯誘因出現破潰來筆者科室治療,破潰約3 cm ×3 cm ×3 cm,基底蒼白伴壞死組織緊密附著,有明顯滲出及異臭味,觸痛不明顯,雙側足背動脈搏動有力,雙下肢血管彩超:雙下肢動脈閉塞2 級,行左足潰瘍清創術后創面縮小好轉出院。患者出院后因左足破潰加重(圖1),創面疼痛,發熱,體溫最高達39℃,伴畏寒、寒戰,以“左足后跟外側破潰5 周,加重伴發熱4 d”再次收治入本院。
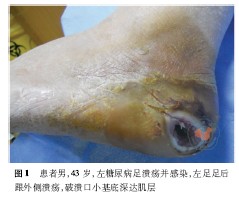
患者糖尿病史7 年余,日常予精蛋白鋅重組賴脯胰島素及阿卡波糖控制血糖,隨機血糖波動在9.0 ~13.0 mmol/L。初步診斷:(1)左糖尿病足潰瘍并感染;(2)2 型糖尿病。
入院后予以查血常規:白細胞27.49 ×109 /L,中性粒細胞23.57 ×109 /L;生化檢查:空腹血糖17.5 mmol/L,糖化血紅蛋白11.3%;創面細菌培養:大腸埃希氏菌(產超廣譜β內酰胺酶菌株)、鏈球菌,血培養陰性。
入院后即予潰瘍創面局部清創引流及每天碘伏紗清洗換藥、頭孢三代及亞胺培南西司他丁鈉治療感染、控制血糖等對癥支持治療。因患者創面疼痛難忍[VAS 視覺模擬評分法(visual analogue scale,VAS)評分8 分],持續發熱(體溫38.5 ~40℃)、高血糖(隨機血糖15.2 ~26.5 mmol/L),潰瘍創面進一步擴大,左足踝部表面大片發黑,伴較多滲液及惡臭,于入院第5 天送手術室行左糖尿病足擴大清創術。
術前患者左足足背動脈可觸及,左足X線片:左踝關節骨關節未見明顯異常,周圍軟組織腫脹、積氣,見左足外踝部皮膚壞死脫落,足后跟外側及足背部紅腫,伴大量滲液(圖2、3);左足內踝部大片皮膚發黑,表面破潰流膿,惡臭明顯(圖4、5)。術中清除皮下壞死組織見踝關節囊及骨質外露,周圍肌腱、跟腱壞死,大量惡臭膿液流出(圖6、7),內外踝貫通積膿伴大量黃黑色壞死組織,踝關節關節囊積膿破壞明顯(圖8、9),予切除壞死組織,暴露至正常組織。術后診斷:(1)左糖尿病足并濕性壞疽;(2)2 型糖尿病。
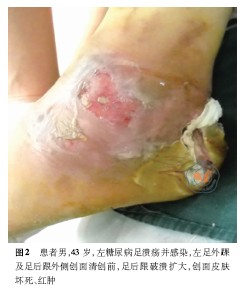
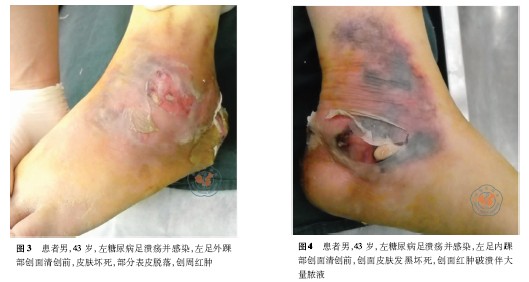
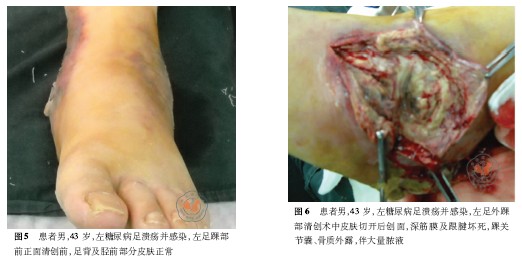
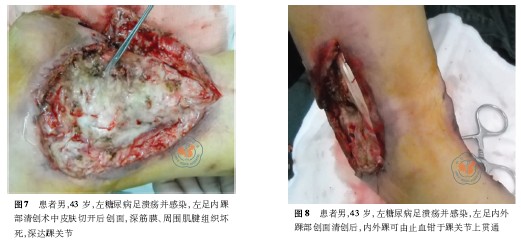
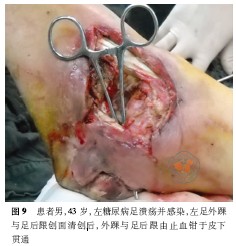
術后第一天患者創面疼痛緩解(VAS 評分4 分)、無發熱、空腹血糖降至12.5 mmol/L。患者術后繼續予抗感染、創面碘伏紗換藥、糾正貧血、控制血糖等治療,創面無明顯惡化及好轉。術后查血管彩超示動脈閉塞:左下肢3 級,右下肢2 級;左足X線片:左踝關節組成骨可疑斑片低密度影,考慮感染所致。骨科會診考慮患者左足壞死明顯伴有嚴重感染建議截肢治療,后轉骨科行左小腿截肢術,傷口愈合拆線后出院。
討論
糖尿病足是患糖尿病后發生的與下肢遠端神經異常和不同程度的周圍血管病變相關的足部感染、潰瘍和(或)深層組織破壞。糖尿病足的基本病理機制是缺血、神經病變和感染,這些因素共同作用導致組織壞死、潰瘍和壞疽。對于糖尿病足多數認為血糖升高是基礎,血管和神經病變是關鍵,足底壓力異常是誘因,合并感染往往使肢體缺血加重而引發糖尿病足壞疽。糖尿病足潰瘍創面伴有大量組織壞死常常可能引起全身炎癥反應,但往往需排除創面感染毒素吸收所致敗血癥的可能性。
該病目前診療方案主要根據潰瘍嚴重程度、血管、感染及神經病變情況,以積極治療感染、重建血運、減輕患肢及傷口壓力為主,通過清創、換藥及護理改善傷口環境。本病例為糖尿病病史不長而合并足部潰瘍的中年患者,臨床表現為起病時潰瘍面積小、Wagner分級低、患肢足背動脈搏動有力,發熱、高血糖、疼痛癥狀突出,局部潰瘍表現為濕性壞死、惡臭明顯,而且創面細菌培養陽性,可排除菌血癥,但潰瘍進展迅速,局部及全身病情兇險,抗感染效果欠佳,常規治療效果不理想時,應該考慮予以外科手術擴大清創引流,及時切除壞死組織治療。
該病例中,筆者起始予創面局部切開引流及清洗換藥,但患足潰瘍快速加深進展至壞疽,盡管最后未能為患者保全肢體,但及時清除創面壞死組織,能有效地減輕患者疼痛及緩解全身炎癥反應癥狀。因此,筆者認為,對于這種起病時潰瘍面積小的糖尿病足病,應當引起警示,發病時盡可能避免感染并注意控制血糖,當感染明顯、高熱高血糖及疼痛癥狀突出時,應當早期外科清創并徹底切除壞死組織,用負壓創傷治療技術促進創面床準備,再行創面植皮修復手術治療。這樣可以有效地緩解患者的癥狀及疼痛,并有可能避免截肢致殘狀況的出現。