患兒,男,7歲,因“間斷頭痛9個月”入院。患兒入院前9個月出現發熱,體溫38 ℃,伴咳嗽、流涕,2 d后出現頭痛,為雙顳部搏動性疼痛,伴眼痛、非噴射性嘔吐及昏睡,無其他伴隨癥狀,每日發作10余次,每次持續數分鐘至數小時,當地醫院診斷“病毒性腦炎”,予抗感染、降顱壓治療2 d后癥狀消失。
入院前5個月患兒“感冒”發熱,又出現頭痛、嘔吐,再次予降顱壓、抗感染治療后緩解;入院前3個月患兒再次出現頭痛、嘔吐發作,不伴發熱,持續時間2~3 h;以后患兒間斷頭痛、嘔吐,2~3周發作1次,多發生于感冒后。患兒為母親第2胎第2產,母親妊娠期有先兆流產史,曾保胎治療,妊娠32周早產,出生體重1500g,新生兒期健康。自幼生長發育遲緩,身高、體重均明顯低于同齡兒,智力、語言、運動發育正常,1歲會走、會說話;約1歲6個月牙齒萌出;平素體質弱,易患感冒;否認家族遺傳史。
體格檢查:神志清,精神反應可,血壓正常;身高89 cm,體重13 kg,頭圍48 cm,雙眼瞼輕度浮腫;心肺腹檢查無異常;皮膚散在直徑2~7 mm咖啡牛奶斑(軀干顯著);特殊面容:三角臉、寬鼻梁、扇風耳,頸短,雞胸,軀干短而寬(坐高40 cm);脊柱側彎,腹部前凸;四肢近端短,遠端大致正常;肘關節、膝關節活動稍受限;顱神經檢查無異常,四肢肌力、肌張力正常,腱反射正常引出,病理征、腦膜刺激征陰性,感覺及小腦共濟檢查無異常,獨行時步態呈鴨步(圖1、圖2)。

輔助檢查:(1)實驗室檢查:血常規、血電解質、肝功、腎功和肌酶正常;血白蛋白:24.2 g/L(正常值:35~55 g/L);尿常規:蛋白(+++),余正常;24 h尿蛋白定量:77 mg/(kg·d)[>50 mg/(kg·d)];血脂四項:總膽固醇9.25 mmol/L(正常值:1.80~5.20 mmol/L)、甘油三酯2.84 mmol/L(正常值:0.40~1.70 mmol/L)、低密度脂蛋白5.86 mmol/L(正常值:0~3.36 mmol/L)、高密度脂蛋白2.09 mmol/L(正常值:1~1.55 mmol/L),均增高;CD系列:CD340.4%(正常值:550%~820%),CD4 7%(正常值:25%~57%),CD8 31.1%(正常值:190%~340%),CD4/CD8 0.2(正常值:1.1~20),CD4和CD4/CD8比值明顯減低;Ig系列大致正常;甲狀腺功能五項正常;尿篩查、血串聯質譜正常;24 h腦電圖:正常;腦血流圖:雙側椎動脈血流速度112~124 cm/s(正常值:75~105 cm/s),雙側大腦中動脈、頸內動脈、大腦前動脈、大腦后動脈血流速度基本對稱;眼底正常,雙眼壓正常。
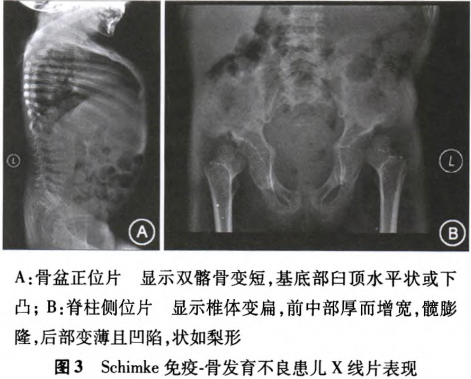
(2)影像學檢查:脊柱側位X線片:椎體普遍變扁,胸腰椎明顯,側位顯示前中部厚而膨隆,后部變薄且凹陷,狀如梨形。椎體前緣不規則,部分椎體上下緣可見骨質缺損(圖3A)。骨盆正位片:雙髂骨變短,基底部增寬,髖臼頂水平狀或下凸(圖3B)。四肢長骨X線片:雙股骨頭細小、碎裂、下移,股骨近端明顯變短,頸干角<90°,雙側髖脫位,假關節形成,股骨遠端改變輕微,肱骨近端可見類似改變,手足等管狀骨形態大致正常。診斷結果:骨軟骨發育異常–脊柱骨骺發育不良。頭顱MRI、磁共振血管造影、磁共振靜脈成像未見異常。
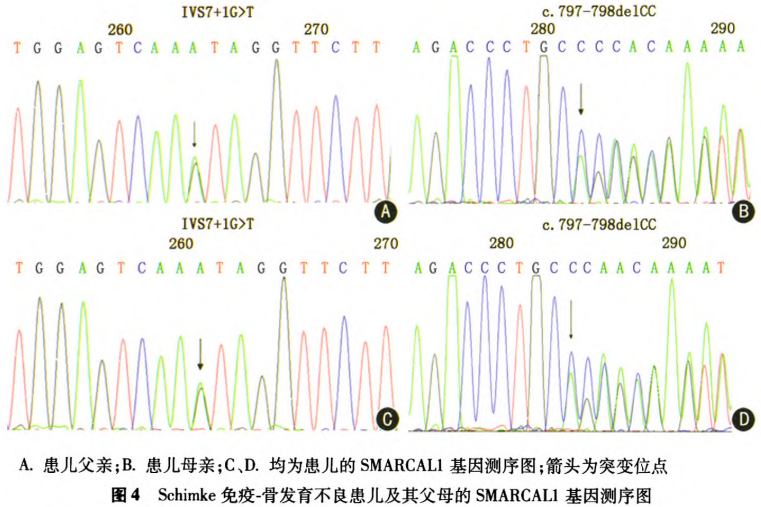
(3)遺傳學檢查:由基因公司進行SMARCAL1基因檢測:取外周靜脈血2 ml,乙二胺四乙酸鈉抗凝,提取基因組DNA,用PCR-Sanger測序技術分析SMARCAL1基因編碼區外顯子和鄰近內含子區突變。該患兒送檢樣本SMARCAL1基因編碼區發現2個雜合突變位點:(1)3號外顯子c.797-798delCC,p.P266QfsX5,兩個堿基的缺失突變導致移碼突變,該突變來自患兒母親;(2)7號內含子IVS7+1G>T,剪接位點突變,該突變來自患兒父親(圖4)。
診療經過:根據患兒三角臉、寬鼻梁、身材矮小、頸及軀干短、脊柱側彎、腰椎前凸、皮膚散在咖啡牛奶斑等特殊體貌;脊柱骨骺發育不良;眼瞼浮腫,蛋白尿、高脂血癥、低蛋白血癥,符合腎病綜合征診斷標準;平素體質弱,易患感冒,CD系列檢查結果提示存在細胞免疫缺陷;綜合上述臨床特點,結合基因學檢查,患兒診斷Schimke免疫-骨發育不良(SIOD)成立。予低鹽、低脂及高蛋白飲食,卡托普利口服降低蛋白尿、保護腎功能及匹多莫德口服調節免疫功能等對癥治療,患兒住院期間未訴頭痛等不適,病情穩定出院。電話隨訪患兒于9歲時因腎功能衰竭死亡。
討論
SIOD是一個多系統受累、進行性加重的罕見常染色體隱性遺傳病,由Schimke等于1971年首先描述,后由Spranger等于1991年命名。本病的發病率約為1:(100~300萬),診斷主要依靠臨床表現,常見臨床表現有:(1)身材矮小:常表現為頸部和軀干短,腰椎前凸和腹部突出;(2)特殊面容:包括寬而塌的鼻梁和大鼻頭,軀干咖啡牛奶斑,部分患者咖啡牛奶斑可延伸至手臂、頸部和腿;(3)脊柱骨骺發育不良:為最常見的影像學異常表現,包括卵圓且扁平的椎體,小而變形的股骨頭骨骺,淺而發育不良髖臼窩;(4)激素耐藥的進展性腎病:幾乎所有SIOD患者有蛋白尿;73%演變為終末期腎病,腎臟病理學為局灶性節段性腎小球硬化;(5)T細胞缺乏:通常為CD4和CD8降低。
近期有學者根據已發表的文獻總結了SIOD臨床表現,除上述外,還有一些少見的異常表現,如近一半患者有嚴重的偏頭痛、短暫性腦缺血發作(TIA)或卒中,受累患者多有熱不耐受。短暫性腦缺血發作或卒中有彌漫性、進行性加重為腦動脈硬化的可能。本患兒有頻繁發作的頭痛,并以此為主訴首診于神經內科,頭痛發作多發生于感染發熱后,結合患兒頭痛的特點,考慮為偏頭痛。SIOD診斷基于臨床特征,分子遺傳學檢測進一步證實診斷;MARCAL1是與SIOD相關的唯一基因突變,約90%的患者可檢測到該致病基因突變。
該基因位于染色體2q34~q36,含有18個外顯子,編碼954個氨基酸,編碼蛋白SMARCAL1表達于全身多個系統,故導致多系統受累,如腎臟、骨骼、胸腺、甲狀腺及血管等。本患兒SMARCAL1基因發現2個雜合突變位點。其中在3號外顯子存在一個微缺失突變c.797-798delCC,該突變導致其編碼的蛋白質的第266個氨基酸殘基由原來的脯氨酸替換為谷氨酰胺,并且因移碼導致終止密碼子提前出現,最終翻譯一個只含有270個氨基酸殘基的截短蛋白,即P266QfsX5,該突變類型尚未見文獻報道。另一個突變位于7號內含子5'端第一個堿基處,即IVS7+1G>T,該突變將導致7號內含子在前體mRNA成熟過程中出現剪接異常,該突變類型目前亦未見文獻報道。家系驗證顯示以上突變分別來自患兒父母,表明這兩個突變位點位于不同的等位基因,符合隱性遺傳規律。
SIOD尚無特異治療,以對癥治療為主。重癥患兒通常在4~8年死亡,常見的死亡原因有感染、卒中、肺動脈高血壓和充血性心臟衰竭、腎功能衰竭等。