以新型生物芯片為代表的自動化智能型醫療技術從腫瘤診療研究走向早期診斷及動態監控等臨床應用,成為精準醫療時代的重要組成。其中,液體活檢是最重要的研究領域之一,在癌癥早篩、預后監測、用藥指導、患者分層等領域均表現出十足的潛力,出現了大批重要臨床結果。
2018年已近尾聲,縱覽一年液體活檢助力精準醫療技術更迭蛻變,美晶醫療微流控芯片ZL技術產品—CellRichTM系統,于年初獲CFDA認證批準,作為循環腫瘤細胞(CTC)檢測新銳技術產品,展露鋒芒,臨床與科研項目開展齊頭并進,未來可期。此外,該系統作為體外免疫診斷領域的一種新的檢測平臺,可以實現各種免疫磁微粒復合物(如細胞、蛋白及核酸等)的特異性分離及捕獲,有望實現液體中外泌體和ctDNA的提取與分析。
液體活檢:應運而生的精準醫療前沿
在精準醫學的時代背景下,液體活檢技術應運而生,與傳統組織活檢相比,液體活檢更能反映腫瘤整體、實時的信息,甚至是全身腫瘤的信息,因此其在腫瘤輔助診斷、療效評估、病情監測及預后評估等方面顯示出獨特的優勢。隨著檢測技術的不斷完善,液體活檢的三大領域CTC、外泌體和ctDNA,在腫瘤精準醫療的臨床應用各放異彩。
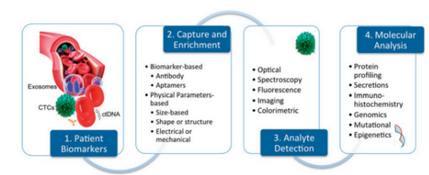
圖1 液體活檢的概念與流程
微流控技術:芯片助力液體活檢
微流控芯片技術是一種在微米或納米尺寸級別下處理或操縱液體的技術手段,由多個不同的操作單元組成,具有通量高、耗時短、耗材少、可控性強等優勢,從而優化檢測過程,實現自動化檢測,是分析化學、細胞生物學、遺傳學等諸多研究領域的重要技術平臺。在生物技術研究領域,微流體技術為生物大分子(如蛋白質),小分子(如核酸)等很多標準生物分子檢測,如酶聯免疫吸附測定(ELISA)、聚合酶鏈反應(PCR)以及逆轉錄PCR(RT-PCR)等提供了全新的自動化技術平臺。微流控芯片技術已經能夠成功地進行液體活檢領域(CTC/ctDNA/外泌體)的分析,并實現成果轉化,走進產品商業化進程,為臨床服務。
下面,我們就來了解一下微流控芯片上的液體活檢技術。
循環腫瘤細胞(CTC): 檢測日趨成熟
循環腫瘤細胞(CTC)是從腫瘤組織脫落進入外周血的各類腫瘤細胞的總稱,是液體活檢領域臨床研究熱度最高的生物標志物。其臨床應用價值逐漸得到臨床承認,并已先后被寫入AJCC癌癥分期手冊(2010、2018)及乳腺癌NCCN指南(2017.V3)。與此同時,隨著微流控技術在液體活檢平臺應用的不斷推進, CTC檢測技術也出現了跨越式的發展。在物理學方法上,自根據腫瘤細胞物理學特性通過膜過濾、密度梯度離心等方法進行細胞的粗分離,已發展到基于微流控檢測技術的力學、介電泳、大小及變形力等多類型高集成度的富集方法;在免疫學方法上,自單純的利用免疫磁珠法富集CTC(anti-EpCAM等正向捕獲法或anti-CD45等負向富集法),發展到在基于微流控納米芯片上實現免疫磁珠法的CTC高效分離。
美晶醫療CellRichTM系統是經過中國國家食品藥品監督管理總局(CFDA)批準的基于微流體芯片的可融合正、負雙向分離方法結合免疫熒光原位雜交技術的檢測平臺,用于惡性腫瘤疾病管理的CTC檢測。并且,隨著檢測技術的不斷改進,CTC檢測的應用已不僅僅局限于計數,美晶醫療在高效捕獲CTC基礎上已建立了多腫瘤標志物、單細胞分析及細胞表達量等相關檢測方法,為進一步分析CTC攜帶的腫瘤基因、蛋白等下游相關組學信息提供技術支持。

圖2 CellRichTM循環腫瘤細胞檢測系統
近年來的臨床研究結果不斷刷新并證實CTC計數在腫瘤患者的輔助診斷、預后評估、療效評估及復發/轉移風險評估的應用價值。2018年權威學術雜志《Journal of Clinical Oncology》上發表的由美國多中心聯合開展的研究結果,入組6081名轉移性去勢抵抗性前列腺癌(mCRPC)患者,以基線和治療后13周后CTC計數和PSA水平的一系列變化作為療效評價指標,結果表明CTC0(基線CTC≥1,13周后CTC=0)和CTC conversion(基線CTC≥5,13周后CTC≤4)這兩個指標可用于評估mCRPC患者療效及預測預后。但是,CTC的應用價值不止于此,基于CTC的下游分析具有更廣泛的前景,如在DNA、RNA、蛋白質水平進行更全面、更深入的分析,為個性化用藥及藥物研發提供指導意義。來自哈佛醫學院的Miyamoto等使用微流控芯片CTC富集技術從前列腺癌男性的血樣本中單獨分離CTC細胞并進行單細胞RNA測序分析,尋找病人內和病人間的異質性,及它們與初期腫瘤樣本的不同之處,揭示了前列腺癌的耐藥機制。Yu等從雌激素受體陽性(ER+)的乳腺癌患者血液中,分離CTC,并通過體外培養建立了細胞系。研究發現CTC與原發腫瘤細胞具有相同的組織學和免疫組化特性;CTCs細胞系基因測序結果顯示CTCs與實體腫瘤保持著一致的遺傳特性,但又擁有一些新的遺傳突變,CTCs存在PIK3CA基因突變和新獲得的突變基因ESR1和FGFR2;進一步對具有多個突變的CTC細胞系進行藥物敏感性實驗發現CTCs對紫杉醇和卡培他濱敏感,對氟維司群、阿霉素和奧拉帕尼耐藥;動物實驗研究發現5株CTCs細胞系中有3株在小鼠上具有致瘤性。以上結果表明CTC體外培養,為藥物篩選提供有效方式。
外泌體(exosome):液體活檢的風口浪尖
外泌體是一種由細胞分泌的,直徑一般為 30-150 nm 的囊泡,攜帶有大量蛋白質、脂質和核酸等源細胞的生物標志物,在血液、唾液、尿液、腦脊液和母乳等多種體液中均有分布。近年來,外泌體被認為是新興的臨床診療的生物標志物,可以揭示來源細胞的生理信息,并直接參與細胞間的信息傳遞、抗原傳遞、蛋白轉運以及 RNA 轉錄等重要的生命活動過程,對疾病的發生機制探索和相關疾病的臨床診斷具有重大的應用價值。
外泌體作為液體活檢的一部分,研究人員利用其物理及生物化學等特性開發了多種分離和純化外泌體的技術方法。傳統常用的外泌體分離方法如超速離心,具有耗時久、通量低及可能損傷外泌體完整性的局限性,適用于大樣本量檢測。進一步分析外泌體表征的方法主要有蛋白印跡法(Western Blotting, WB)、酶聯免疫吸附法(Enzyme-linked immunosorbent assay, ELISA)、電泳、比色、qPCR等。近年來,基于過濾、免疫親和、免疫磁珠等原理,利用微流控技術在生物芯片捕獲并分析高純度外泌體的方法,在靈敏度、自動化及檢測通量等多方面展露優勢。但是,與CTC檢測相比,基于微流控芯片技術的外泌體檢測平臺還未有商業化平臺,眾多科研成果待轉化。
另外,基于免疫的方法一直是分離外泌體的重要分支。研究者He等人開發了一種微流控方法,將磁珠集成到芯片上,用于多種外泌體亞群的免疫磁微粒捕獲和外泌體靶向蛋白的熒光分析。所開發的帶網孔的PDMS芯片巧妙采用多步免疫磁微粒法,如圖3所示,第一步,用抗體標記的磁珠捕獲目標外泌體;第二步,添加裂解緩沖液,將蛋白質釋放到微通道中,用抗體標記的磁珠捕獲這些蛋白質;第三步,采用熒光抗體技術分析蛋白質。該免疫磁珠結合微流控技術的方法,僅需30ul樣本,外泌體的捕獲效率高達99.9%,而且可以方便地制備透射電鏡表征樣品,這是超速離心等傳統方法無法實現的,為微量樣本的外泌體分離和分析提供了新的方式。Vaidyanathan等人開發一種通過引入電場來改善特定外泌體的免疫靶向捕獲的微流體裝置,與常規基于流體力學分離外泌體的微流控系統相比,該技術大大提高了外泌體捕獲率。
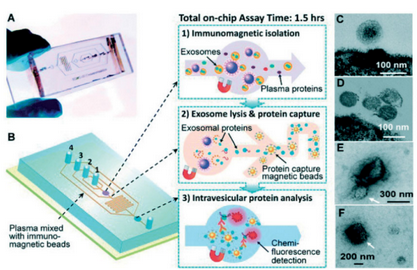
圖3 基于免疫磁微粒的微流控外泌體捕獲與分析平臺
目前,美晶研發團隊利用生物芯片技術,結合微流體和過濾兩種方法,將由多孔硅納米線組成的纖毛微柱整合到微流控芯片上,形成微流控過濾系統(圖4)。通過優化微柱的幾何形狀、分布位置與密度,為外泌體提供充足的結合位點,且不影響微流體通道內液體流動,在10分鐘內實現外泌體的高效捕獲。然后通過溶解多孔硅納米線,釋放外泌體,實現完整外泌體的高純度回收。以上基于微流控技術分離外泌體的方法,在外泌體的純度、回收率、生物活性等方面具有突出優勢,且具有樣本需求量較少的優點,與常規傳統方法相比更適用于微量樣品分析,有望被廣泛應用于未來無創精準診療中。當然,當前基于微流控的外泌體分離方法仍處于實驗研究階段,還有待深入研究,以供臨床應用。
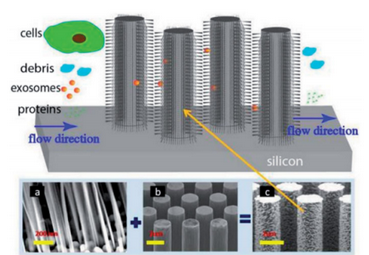
圖4有纖毛的微柱陣列分選外泌體示意圖
由于外泌體同循環腫瘤細胞一樣,具有豐富的內含物,對其進行定量及定性分析對臨床意義重大。目前,由于外泌體中的mRNA、lncRNA等RNA,含量較低且不穩定,其臨床研究集中于mircoRNA。Jin等使用miRNA-seq對腺癌患者、鱗癌患者及健康人群進行外泌體來源的miRNA分析發現,AC或SCC特異性的腫瘤來源的外泌體miRNA的獨特性質,miR-181-5p、miR-30a-3p、miR-30e-3p和miR-361-5p具有腺癌特異性,miR-10b-5p、miR-15b-5p和miR-320b具有鱗癌特異性,并對其診斷準確性進行了驗證,表明外泌體miRNA可用于非小細胞肺癌的早期診斷。Ogata-Kawata等人比較了88例結腸癌患者和11例健康對照組血漿中的外泌體的7種miRNAs(let-7a、miR-1229、miR-1246、miR-150、miR-21、miR-223和miR-23a)表達,發現它們在結腸癌患者中的表達顯著高于健康對照組;對于I期結腸癌患者,miR-23a和miR-1246同樣具有高度的敏感度,分別為95%和90%,而CA199和CEA的敏感度分別只有10%和15%,表明外泌體miRNA可用于結直腸癌輔助診斷。
循環腫瘤核酸(ctDNA):檢測任重道遠
ctDNA 即循環腫瘤DNA(Circulating tumor DNA),是腫瘤細胞在壞死、凋亡后釋放的一種游離DNA,具有和惡性腫瘤相關的分子生物學特征。ctDNA檢測具有無創、快速、全面等特點,且能克服組織標本局限性,因此對ctDNA的定量和基因分型分析對腫瘤患者診斷和病情監測具有重要臨床意義。
但是,在腫瘤患者外周血循環DNA中,真正來自腫瘤細胞的DNA含量非常低,傳統的檢測方式是研究者通常需要通過PCR的方式擴大其分子數量,也稱芯片式數字PCR法。Sefrioui等人評估了芯片式數字PCR方法是否可用于分析癌癥患者的循環DNA,他們入組34名轉移性結直腸癌患者進行致病基因 K-ras基因定量分析,研究結果表明該方法用于患者樣本ctDNA的定量分析,雖然檢測流程相對簡單且耗時短,但同時其額外的步驟需要相應的配套設備來配合完成,因此對檢測條件有一定的要求。并且,近年來研究發現,單純基于生物學的方法很難進一步提高檢測的靈敏度,且受限于手工操作誤差大,而微流控芯片技術的快速發展,為進一步提高檢測靈敏度與自動化提供新策略。目前,已有利用磁場,在微流控光學芯片系統中實現cfDNA的快速分離與特異性分析。Dias等人開發了一種基于磁阻傳感器陣列的生物芯片上,利用堿基互補配對原理,通過磁珠標記靶向序列,在微流體通道上實現cfDNA靶向序列多步富集和檢測。Cai等人開發了一種微流體光學系統(圖5),實現人外周血cfDNA的自動化分離與分析。該系統由多層結構組成,首先對血液進行過濾,然后通過磁珠法富集cfDNA,再利用熒光標記目的基因,通過光學系統進行分子分析。此類既不需PCR過程,又可實現目標基因的檢測,非常適用于臨床樣本ctDNA檢測推廣。美晶醫療CellRichTM循環腫瘤細胞檢測系統,是基于微流控芯技術及免疫磁珠富集法的液體活檢平臺,具有集成性、分辨率高、分析速度快、高通量、物耗少和安全廉價等優點,未來,對基于該平臺的液體活檢技術進行適當的延伸,同樣將在ctDNA高效捕獲、分析領域應用具有廣闊的前景。
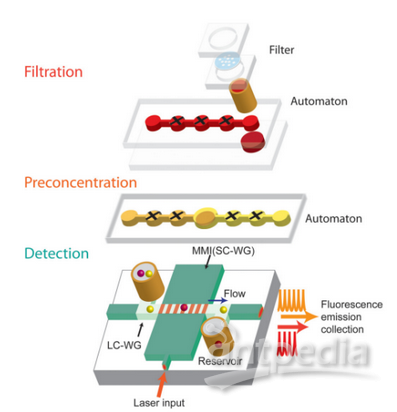
圖5 微流體光學系統結構示意圖
目前,ctDNA的臨床應用方向主要集中于靶向用藥指導,如血液樣本EGFR基因檢測指導晚期非小細胞肺癌患者用藥。近年來一項來自日本及歐洲的多中心研究結果提示,對歐洲和日本的晚期NSCLC患者ctDNA檢測EGFR突變狀態評估研究,發現血漿和組織中的EGFR突變的一致性高達89%,基于這些大量的真實臨床數據,目前認為當腫瘤標本不可用或無法獲取時,對血漿樣本進行ctDNA EGFR突變分析,是一個可行的方案。另外,依據2018年美國臨床腫瘤學會(ASCO)和美國病理學家協會(CAP)聯合發布的綜述文章,表明ctDNA在臨床應用范圍非常廣泛,涉及到腫瘤早期篩查、療效監測、用藥基因檢測及復發/轉移風險評估等。但是,目前臨床有效性數據有限,臨床實用性還需建立在技術精準及進一步大數據研究基礎上。
結語:液體活檢作為一項具有顛覆性的新興生物醫學工程前沿,承載了精準醫療的希望。基于微流控芯片的液體活檢技術,正在實現臨床轉化,成為腫瘤個性化診療的重要手段。2018年2月9日,國家食品藥品監督管理總局(CFDA)正式審核通過寧波美晶醫療技術有限公司(NanoLite Systems)自主研發的新一代CellRichTM自動化循環腫瘤細胞捕獲設備。據悉,該設備是目前國內唯一通過國家認證的基于免疫磁篩選微流控芯片ZL技術的自動化雙模式循環腫瘤細胞篩選設備,臨床數據顯示,可實現人體外周血中腫瘤細胞(CTC)的精準捕獲。當然,液體活檢要廣泛進入臨床應用,不僅需要高精準的檢測技術平臺,還需建立在進一步大量和細化臨床研究的基礎上,形成相應的檢測標準與規范。美晶醫療作為液體活檢技術領先的服務商,將以平臺為基礎,進一步全力推進液體活檢領域中外泌體及ctDNA檢測技術等相關領域開發及應用,提供全面的液體活檢解決方案,為加速中國精準醫療時代的到來貢獻力量。
參考文獻:
1. Tadimety A, Closson A, Li C, Yi S, T. Shen, Zhang JXJ. Advances in Liquid Biopsy On-Chip for Cancer Management: Technologies, Biomarkers, and Clinical Analysis. Critical Reviews in Clinical Laboratory Sciences. 2018, 55:140-162.
2. Heller G, McCormack R, Kheoh T, et al. Circulating Tumor Cell Number as a Response Measure of Prolonged Survival for Metastatic Castration-Resistant Prostate Cancer: A Comparison with Prostate-Specific Antigen across Five Randomized Phase III Clinical Trials. Journal of Clinical Oncology. 2018, 36(6):572-580.
3. Miyamoto DT, Zheng Y, Wittner BS, et al. RNA-Seq of single prostate CTCs implicates non canonical Wnt signaling in antiandrogen resistance. Science. 2015, 349:1351-1356.
4. Yu M, Bardia A, Aceto N, et al. Cancer therapy. Ex vivo culture of circulating breast tumor cells for individualized testing of drug susceptibility. Science. 2014, 345(6193):216-20.
5. Jin X, Chen H, Fei S, et al. Evaluation of tumor-derived exosomal miRNA as potential diagnostic biomarkers for early stage non-small-cell lung cancer using next-generation sequencing. Clin Cancer Res. 2017, 23(17):5311-5319.
6. Ogata-Kawata H, Izumiya M, Kurioka D, et al. Circulating exosomal microRNAs as biomarkers of colon cancer. PLoS One. 2014, 9(4): e92921.
7. Chen G, Huang AC, Zhang W et al. Exosomal PD-L1 contributes to immunosuppression and is associated with anti-PD-1 response. Nature . 2018, 560(7718):382-386.
8. Martin R, Koichi H, Baohui H, et al. ctDNA Determination of EGFR Mutation Status in European and Japanese Patients with Advanced NSCLC: The ASSESS Study Journal of Thoracic Oncology. 2016, 11(10): 1682-1689.
9. Merker JD, Oxnard GR, Compton C, et al. Circulating Tumor DNA Analysis in Patients With Cancer: American Society of Clinical Oncology and College of American Pathologists Joint Review. Journal of clinical oncology. 2018, 36(16):1631-1641.
GeneCentricTherapeutics周三宣布完成800萬美元C輪首輪融資,以支持其GenomicsNext循環腫瘤DNA(ctDNA)液體活檢平臺的推出和商業化。此次融資由HatterasV......
由于無法對蛋白實現擴增,因此在單細胞多組學的研究中,單細胞蛋白質組學是最具挑戰的研究,近年來已取得突飛猛進的進展。除了質譜儀檢測靈敏度的提升,在前端取樣、預處理和分離方面的巨大進步是重要因素,這和微流......
工業和信息化部辦公廳近日印發了《第一批先進適用技術名單》。經過自主申報、初審推薦、專家評審和公示等嚴格程序,最終確定了涵蓋有色、化工、通用機械、輕工、電子等多個行業的111項先進適用技術。這些技術不僅......
近日,廣東省特種設備檢測研究院珠海檢測院申報的《檢驗檢測技術、專利、標準聯動創新指南》地方標準,經專家審議、現場答辯,獲珠海市市場監管局批準立項。為了保障檢驗檢測質量,提升檢驗能力,發揮標準化作用在檢......
近日,中國科學院大連化學物理研究所研究員樸海龍與中山大學腫瘤防治中心鞠懷強教授、徐瑞華教授團隊合作,建立了基于血清脂質組學的胃癌診斷與預后分型高性能機器學習模型,能夠根據病人的血清脂質組學數據對病人是......
10月10日,2024中國汽車工程學會越野車技術分會第十六屆學術年會暨特種車輛大會在長沙舉行。大會已舉辦16屆,本屆以“匯智、融通、協創、勇拓”為主題,設置高峰論壇、展覽展示、論文證書頒發等環節。大會......
關于征集“集成芯片前沿技術科學基礎”重大研究計劃2025年度項目指南建議的通告國家自然科學基金重大研究計劃“集成芯片前沿技術科學基礎”2025年度項目指南建議征集已通過科學基金網絡信息系統(https......
在生命科學領域,基因編輯技術尤其是CRISPR/Cas9系統的出現,為科學研究帶來革命性突破。這項技術改變了人類對基因的認知,重新定義了自然選擇與人工干預間的界限。老百姓眼中,基因編輯可能也是類似于“......
9月26日至27日,國家能源水電工程技術研發中心2024年數智水電技術交流論壇在長沙舉辦。論壇現場。主辦方供圖論壇以“數智水電,賦能發展”為主題,圍繞數智水電前沿技術及發展趨勢進行研討,包括5場主旨報......
9月27日,國防科技大學聯合湖南省人民政府、軍事科學院、中國電子信息產業集團有限公司、中國兵器裝備集團有限公司舉辦的第二屆國防科技高地論壇主論壇在長沙舉行。論壇現場。王昊昊攝論壇由國防科技大學牽頭發起......