破骨細胞前體細胞的Lkb1缺陷不會誘導成骨腫瘤樣表型
破骨細胞抗酒石酸酸性磷酸酶(TRAP)染色發現,Ctsk-CKO小鼠的骨膜、骨內膜和松質骨的破骨細胞數量增加。研究人員還利用Ctsk-CKO和Ctsk-Ctrl小鼠的骨髓細胞分化為破骨細胞。TRAP活性定量顯示,來自Ctsk-CKO骨髓細胞的破骨細胞形成增加(圖3),說明Ctsk-CKO小鼠的骨量增加并非因為再吸收受損。其他實驗排除了Ctsk-CKO小鼠的成骨腫瘤樣表型與破骨細胞功能改變有關。
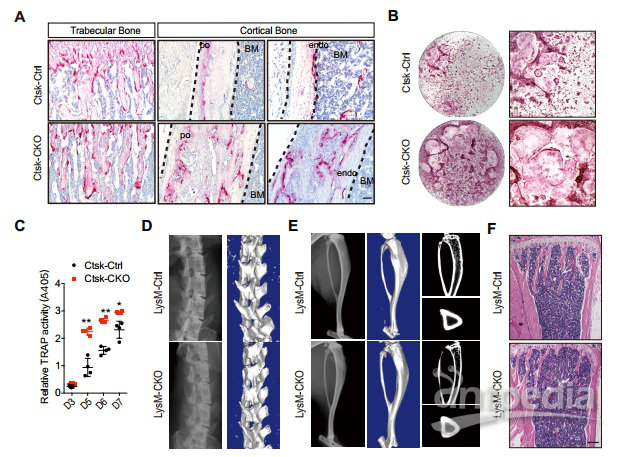
圖3. 破骨細胞前體細胞缺失Lkb1不會造成成骨腫瘤樣表型
Ctsk-Cre成骨間充質細胞是成骨腫瘤的潛在來源
細胞譜系追蹤顯示Ctsk-Cre陽性LysM-Cre陰性細胞群位于致密骨的骨膜內(圖4)。隨著年齡增長,Ctsk-CKO小鼠的Ctsk-Cre陽性細胞不斷擴張填滿了脛骨的致密骨。20周齡前,GFP陽性細胞形成脛骨Ctsk-CKO小鼠的骨樣腫瘤,暗示成骨腫瘤來自LKB1缺失本身。

圖4. Ctsk-Cre骨膜間充質干細胞是成骨腫瘤的新型潛在來源
接著研究人員分析了Ctsk+細胞的通用干細胞標記表達情況,發現Sca1、CD24、CD44、CD49f 和CD146都有表達。隨后采用賽業生物(Cyagen)干細胞定向誘導技術,體外觀察骨膜Ctsk+細胞的分化潛能,證明它們可以分化為成骨細胞和軟骨細胞,以及表達相應的分化標志物。換句話說,Ctsk可定義為一群間充質干細胞。
LKB1抑制Ctsk+骨膜間充質干細胞的自我更新和成骨分化能力
鑒于Ctsk+骨膜間充質干細胞的角色,這項研究首次發現Lkb1可以抑制這些細胞的自我更新能力以及成骨分化能力。
為了驗證,Lkb1缺陷是否足以驅動正常小鼠的成骨腫瘤形成。研究人員分別將對照小鼠和Ctsk-CKO的骨膜源性細胞進行裸鼠皮下注射移植。8周后,HE染色和共聚焦成像顯示,Ctsk-CKO組骨樣基質的細胞和核表現出腫瘤異型性和腫瘤形成特征。
隨后,抑制mTORC1信號可以改善Ctsk-CKO小鼠腫瘤進展,并阻止異種移植模型的腫瘤生成
【總結】
本研究證明了骨膜Ctsk+細胞的LKB1缺失導致成骨腫瘤樣表型,介導途徑為mTORC1的活動增加,澄清了Lkb1在人類骨肉瘤生成中的作用。此外,擴展了Ctsk+細胞的定義,即它們不僅是一類新型骨膜間充質祖細胞,而且還是骨肉瘤的來源。
骨髓瘤治療可以靶向多條通路的聯合療法以期取得協同效應,例如,理論上采用雷帕霉素結合抗VEGF療法,治療LKB1損傷的骨肉瘤患者。LysM+細胞缺失Lkb1后不會導致致密骨腫瘤形成,說明破骨細胞沒有參與Lkb1相關骨肉瘤發病機理。而實際上,Ctsk-CKO和LysM-CKO小鼠都表現出破骨細胞形成(圖3),Ctsk-CKO小鼠富含大量破骨細胞和破骨細胞前體細胞,意味著Lkb1可能在破骨細胞生成方面起到一定作用,未來,研究人員準備進一步調查Lkb1影響破骨細胞生成的具體角色。
原文檢索:Lkb1 deletion in periosteal mesenchymal progenitors induces osteogenic tumors through mTORC1 activation